3 تعاميم أصدرتها «الصحة ووقاية المجتمع»
تحذير من دواء لعلاج التليّف الرئوي ومقوٍّ جنسي.. وتعليق ثالث للسكري
أصدرت وزارة الصحة ووقاية المجتمع، ثلاثة تعاميم إدارية لإضافة تحذير على مستحضر صيدلاني لعلاج التليّف الرئوي، قد يتسبب في حدوث إصابات خطرة في الكبد، وتعليق تسجيل مستحضر صيدلاني آخر لعلاج السكري لعدم مطابقة بعض التشغيلات للمواصفات المعتمدة، والتحذير من مكمل غذائي ومقوٍّ جنسي، لاحتوائه على مادة دوائية غير معلن عنها تسبب الانخفاض الحاد في ضغط الدم. وأكد الوكيل المساعد لسياسة الصحة العامة والتراخيص رئيس اللجنة العليا لليقظة الدوائية، الدكتور أمين حسين الأميري، حرص الوزارة على متابعة التحذيرات والتوصيات الواردة من شركات تصنيع الدواء والهيئات العالمية للدواء، وذلك في إطار جهود الوزارة لتحقيق نظم وتدابير الحماية المجتمعية من مخاطر التزييف الدوائي، والحرص على تحقيق الوقاية والسلامة للمرضى والمجتمع.
|
منتَج يستخدم كمكمل غذائي ومقوٍّ جنسي يحتوي على مادة دوائية غير معلن عنها. |
وذكر أن الوزارة أبلغت من قبل شركة مصنّعة بإضافة تحذير لها على المستحضر الصيدلاني Ofen nintedanib، الذي يستخدم لعلاج التليّف الرئوي، إذ إنه يتسبب في حدوث إصابات خطرة في الكبد، ويجب على ممارسي الرعاية الصحية فحص ترانس امينيز والبيليروبين في بداية العلاج خلال أول ثلاثة أشهر من العلاج دورياً، وبعد ذلك في كل زيارة للمريض، أو كما هو محدد سريرياً، كما ينصح بتقليل الجرعة أو أخذ العلاج المناسب عند ارتفاع الترانس امينيز، علماً بأن المنتج مسجل في إدارة الدواء بوزارة الصحة ووقاية المجتمع.
ولفت إلى أن الوزارة أوصت ممارسي الرعاية الصحية بأخذ الحيطة والحذر عند صرف هذا الدواء لمرضاهم، علماً بأنه آمن للاستخدام ولم يتم سحبه من الأسواق، وهذه التحذيرات تضاف للنشرة الدوائية فقط.
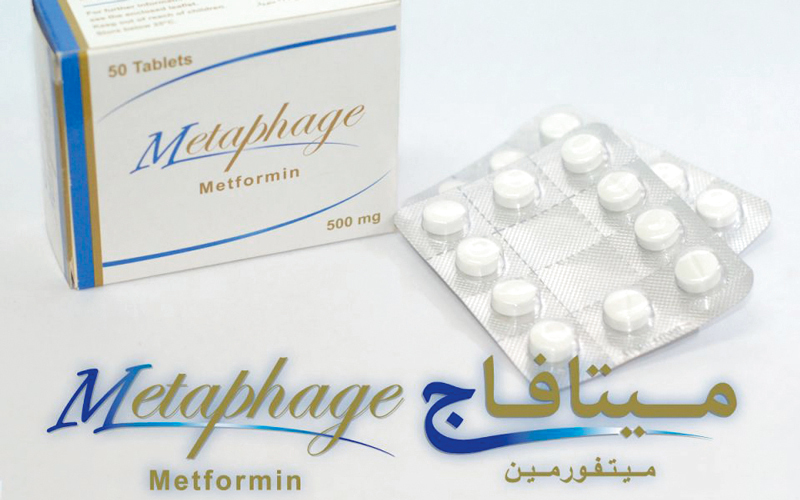
وأضاف الأميري أنه تقرر إصدار تعميم بتعليق تسجيل المستحضر الصيدلاني Metaphage 500mg tablet للشركة المصنعة الكويتية السعودية، بناءً على ما ورد للوزارة من مجلس الصحة لدول مجلس التعاون بخصوص تعليق تسجيل هذا المنتج المستخدم لعلاج مرض السكري، وذلك بناءً على نتائج دراسات التحليل المخبرية لعدد من التشغيلات، التي بينت عدم مطابقتها للمواصفات المعتمدة، كما تمت دراسة التكافؤ الحيوي، وبيّن تصميم الدراسة أنه غير مناسب، ولا يتطابق مع الشروط المعتمدة للدراسات المتعلقة بنوعية هذه الأدوية، مشيراً إلى توصية اللجنة الخليجية المركزية للتسجيل الدوائي، بتعليق المستحضر، وعمل دراسة تكافؤ حيوي للمستحضر تحت إشراف الهيئة العامة للغذاء والدواء بالسعودية، علماً بأن المنتَج مسجل في وزارة الصحة ووقاية المجتمع. وبيّن أنه تقرر تعليق تسجيل المستحضر، لحين الانتهاء من التحقق من جودة المنتج، كما يجب على المورد سحب جميع التشغيلات للمستحضر من القطاع الصحي العام والخاص، مؤكداً أن على جميع ممارسي الرعاية الصحية عدم استخدام المنتَج إن وجد لديهم، وعلى الصيدليات كافة التوقف عن صرفه وإعادته للمورّد.
وأوضح الأميري أن إدارة الغذاء والدواء الأميركية أبلغت الوزارة بخصوص المنتجRhin 69 Extreme 5000 capsulate الذي يستخدم كمكمل غذائي ومقوٍّ جنسي للرجال، إذ أظهرت التحاليل احتواءه على مادة دوائية غير معلن عنها اسمها Tadalafil، علماً أنها تسبب الانخفاض الحاد في ضغط الدم قد يصل إلى مستوى خطر، ويمكن أن تشكل خطراً على المصابين بأمراض القلب والسكري أو ارتفاع الدهون، خصوصاً الذين يتناولون أدوية تحتوي على النترات، لذا أصدرت الوزارة تعميماً للمنشآت الصحية والصيدلانية الحكومية والخاصة لاتخاذ الإجراءات لسحب المنتَج من الأسواق، ومنع تداوله واستيراده في حال توافره، علماً بأن المنتج غير مسجل في إدارة الدواء بالوزارة.
![]() تابعوا آخر أخبارنا المحلية والرياضية وآخر المستجدات السياسية والإقتصادية عبر Google news
تابعوا آخر أخبارنا المحلية والرياضية وآخر المستجدات السياسية والإقتصادية عبر Google news